文章概要:作者山脚下的蚂蚁,描述了方案偏离数据统计分析的样例,再到相关数据的收集流程、最后到统计分析对数据的要求等
开篇声明:1:以下内容非原创,转自微信公众号山脚下的蚂蚁《6 方案偏离数据收集流程和常见数据问题》,如有侵权,可联系删除
2. 以下观点,仅代表作者个人观点,请带着质疑的态度去阅读,如有问题,欢迎评论区留言或直接联系作者
方案偏离数据收集流程和常见数据问题
前言
今天看到了一篇不同角度的关于PD的文章https://mp.weixin.qq.com/s/qJrb6vBgkoVNBhALGUsm8g,写得很好很详细,大家可以一起学习下。
—————————————————
最近有一点忙,好久没写了,抱歉。。。写点什么呢?写一下最近的问题和感慨吧。
最近一个项目的方案偏离遇到了很多的数据问题,经过了数轮的邮件沟通依然无效,让我一度怀疑这个 global CRO 相关人员的资质和经验。
既往也经常会有一些资深的DM、Programmer、统计师甚至PM问我关于方案偏离的流程,那么我这里就借机会来给大家科普一下我眼里的方案偏离数据的收集流程以及常见的数据问题。不同的 CRO 或者 Sponsor 的流程可能有所出入,但宗旨基本一致。如有纰漏,欢迎批评指正哈~
正文
以终为始,我们先来说一下方案偏离(Protocol Deviation,下简称PD)的最后的数据分析或者呈现。(方案偏离或方案违背(Protocol Violation)从统计分析的角度都是一回事儿,但有些人认为两者性质不一样,方案违背更严重,有故意或恶意的嫌疑,故使用“方案偏离”字眼比较中性一些)
1. 数据呈现
PD 数据的呈现一般是至少一个列表;如果PD数量较多,可以再提供一个表格。
表格:通常是基于Safety Set,对Major/Important/Severe PDs 或者 all PDs 按照具体的分类和子分类汇总各个治疗组的人数和百分比。如果PDs数量较少,一个列表就看清楚问题了,不出表格也是Okay的,比如Phase 1或者BE的一些项目。(当然不管PDs数量多少或者有无,均提供一个表格也是Okay。)
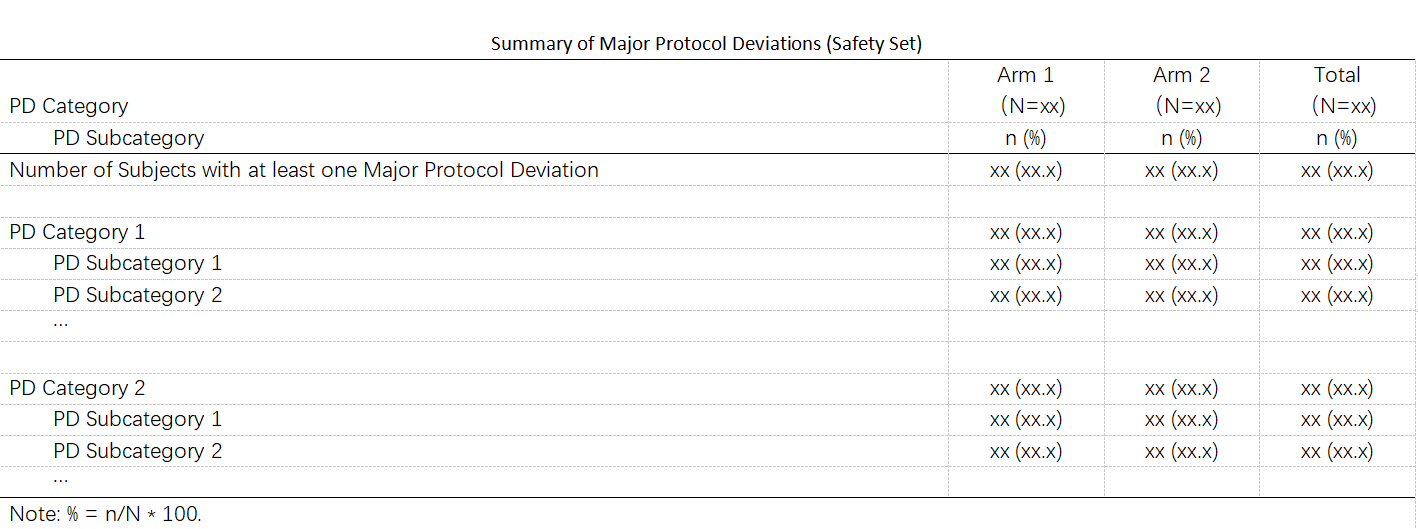
需要注意的是,分析可能需要根据具体的计划来调整。比如,有的申办方可能定义:一级分类、二级分类、和三级分类然后是具体的描述以及严重程度,那么这个时候汇总可能也需要调整到三级分类。因为此时仅一级和二级分类无法提供足够有效的信息。
列表: 通常是基于Safety Set,至少包括受试者编号、PD分类和子分类(或者1-3级分类)、PD描述、以及严重程度等信息。
2. 方案偏离数据流程
第一步 计划 (PD Plan)
在临床启动前,定义方案偏离的分类、子分类以及严重程度等(下简称PD Plan)。某CRO是将其包括在Medical Monitior Plan中,由MM来起草;某Sponsor是撰写了一份独立文件PD Plan,由PM来起草。你所在单位是谁来撰写?欢迎留言交流。
方案偏离的严重程度:
-
大多为二分类,比如Major/Minor, or Important/Non-important; -
也有的CRO或者Sponsor用三分类,比如Mild/Moderate/Severe。 -
无法确定的其严重程度的条目,在计划里严重程度定为TBD;有了具体数据后,根据实际情况来考量其严重程度。
第二步 临床实施
方案偏离分类的计划里可以提前划分一下职责,哪些条目是通过Medical Review, CRA Monitor, DM Review or SAS Programming来发现,均可在PD Plan里进行规定。(对于Phase 1 非肿瘤项目或者BE项目,样本量小,数据量小,试验周期短,PDs的收集建议可不用通过SAS编程收集。)
依照这个计划的分类,各个function进行方案偏离的收集和上报。PM/DM可能会对各个function收集上来的PD进行reconcilation和去重,然后找Medical,Statistician进行审阅。
在数据库锁定前一般会开数据审核会(有的公司是DM lead,有的公司是统计Lead):
-
数据审核会上可以对有争议的PD(主要是针对严重程度)和各个function以及PI进行讨论,最终定稿PD listing。 -
同时讨论方案偏离(主要是重大方案偏离)对分析人群的影响(比如是否纳入符合方案分析集PPS),从而将分析人群定稿。
定稿后的PD listing将最终传输给统计编程进行数据分析。
3. PD数据常见数据问题
-
PD的一级/二级分类、编号等信息保持和PD plan一致: -
尽量采用下拉选择的方式来填写,尽量避免人工手动录入。 -
PDs间的一致性:相同的PD应该归属相同的PD分类和严重程度。 -
PD的描述: -
尽量描述受试者相关的客观事实,尽量不要掺和意见以及处理措施; 针对PD 的意见和处理措施可以描述单独描述;比如CAPA,CRA/PI针对PD的看法或者action taken, 或者项目组为预防take的action可以和PD的描述分不同的列进行描述。 -
建议PD描述添加访视信息或者入组时间等相对时间(方便把故事讲清楚)。 -
PD描述不宜过长(比如不超过200个字符),不然将来统计编程生成的listing会非常大。 -
PD的严重程度: 和PD Plan保持一致。 -
受试者编号:中心层面的PD受试者编号统一为空,或者NA;受试者层面的PD,受试者编号不能为空。 -
删除线不管用,需要删除行或用flag 标识。 -
最后定稿的PD listing 严重程度列无TBD。 -
避免重复上报相同的PDs。
前文我抱怨的Global CRO提供的PD listing基本出现了上述所有的数据问题,其PD的描述最长能达到3300+个字符。他们的PD数据已经完全脱离了PD Plan的控制,各种不一致。关键是数轮的沟通和修订,始终未得到较好的解决。我真的是无语至极。
4. PD 数据讨论
对于数据展示,我们一般都是Safety Set, 也就是用药的受试者;而PD在收集的时候是分为中心层面和受试者层面的;中心层面的PD(比如药物保存超温)一般受试者编号为空;那么中心层面的数据是否需要纳入SDTM DV 以及分析数据集ADDV呢?
下为个人理解,供参考:
-
中心层面的PDs是无法纳入相应表格和列表的,因为分析是基于某个人群来展示的,比如Safety Set。 -
因为分析数据集是为其分析表格和列表准备的,故中心层面的PDs不用纳入分析数据集ADDV。 -
中心层面的PDs也无需纳入SDTM DV,不然Pinnacle 21 validation会report问题。所有PDs均录入在相应的数据库以及source document,将来CDE核查也是针对这些记录进行,而非SDTM。综上,我认为SDTM DV 亦无需包含中心层面的PDs。(如有不同理解,欢迎私信讨论哈~)
那么在CSR撰写的时候,如何对中心层面的PD进行描述呢?如果需要描述,个人建议Medical Writer关注一下finalized PD listings 中心层面的PD,然后Mannual review and report。(个人见解,可能有失偏颇哈,欢迎私信讨论)
结语
对于PD数据的收集,不同的单位有不同的流程,但宗旨大体一致。
大家如何不同的理解和做法,欢迎私信来沟通和讨论哈~
如有纰漏,也欢迎批评指正~
最后给大家一句寄语:即便是行业大拿,大多也是摸着石头过河累积的经验,极少人是统计理论基础扎实,说话绝对正确。希望大家带着质疑的态度,来阅读和聆听(包括我的文章),然后根据自己的实际情况内化为自己的知识和技能。
完结











0条评论